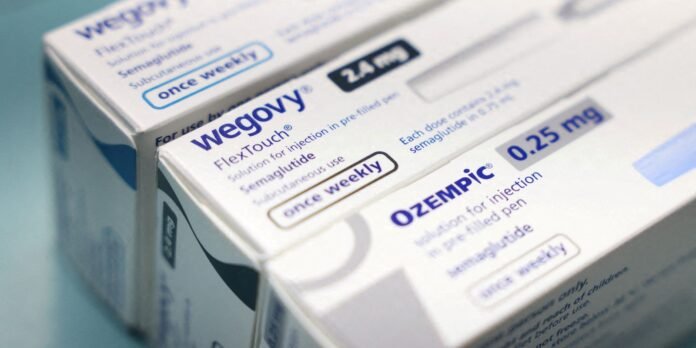
A Anvisa anunciou nesta segunda-feira (6) um conjunto de medidas para reduzir riscos e reforçar o controle sanitário de medicamentos injetáveis agonistas do receptor GLP‑1, conhecidos como canetas emagrecedoras.
O plano alvo irregularidades na importação de Insumos Farmacêuticos Ativos (IFAs) e na manipulação de semaglutida, tirzepatida e liraglutida por farmácias de manipulação. Segundo a agência, a importação de IFAs tem sido incompatível com a demanda do mercado nacional: no segundo semestre de 2025 foram importados 130 quilos de insumos, volume suficiente para a preparação de cerca de 25 milhões de doses.
Em 2026, a Anvisa realizou 11 inspeções em farmácias de manipulação e empresas importadoras. Essas ações resultaram na interdição de oito estabelecimentos por problemas técnicos e falhas no controle de qualidade. A agência também relatou aumento de notificações de eventos adversos e identificou uso off‑label desses produtos, incluindo indicações para emagrecimento sem necessidade clínica. Em fevereiro, foi emitido um alerta sobre risco de pancreatite associado às canetas.
Riscos identificados incluem produção sem previsão de demanda individualizada, falhas em processos de esterilização, controle de qualidade inadequado, uso de insumos sem identificação de origem e composição, uso indevido de nomes comerciais e comercialização de múltiplos produtos sem registro. A Anvisa enfatiza que padrões rigorosos de esterilidade e pureza são essenciais para injetáveis manipulados.
Desde janeiro, a agência publicou dez ações proibindo a importação, o comércio e o uso de produtos irregulares que contenham agonistas de GLP‑1.
Eixos estratégicos do plano de ação
A Anvisa estruturou o plano em seis eixos estratégicos:
– Aprimoramento regulatório: revisão da Nota Técnica 200/2025 para orientar importação, manipulação e controle sanitário de IFAs de agonistas de GLP‑1, incluindo rastreabilidade, critérios de qualidade, qualificação de fabricantes e testes mínimos de controle; revisão da RDC 67/2007, que disciplina boas práticas de manipulação; e fortalecimento de medidas cautelares para suspensão de autorizações de funcionamento em risco iminente.
– Monitoramento e fiscalização: intensificação de inspeções em importadoras, farmácias de manipulação e clínicas de estética; busca ativa de eventos adversos em serviços de emergência, hospitais e clínicas; uso do sistema VigiMed para notificações; aprimoramento da matriz de risco para controle de importação de IFAs; e ampliação de ações para impedir a entrada de produtos irregulares no país.
– Articulação institucional, federativa e internacional: criação de acordos de cooperação técnica e de grupos de trabalho com entidades médicas e órgãos de controle; ações de informação e capacitação com o Sistema Nacional de Vigilância Sanitária; e cooperação com agências reguladoras internacionais.
– Ampliação da oferta de produtos registrados: priorização da análise de pedidos de registro — a Anvisa informou que há 17 pedidos de registro de canetas em andamento — visando aumentar a oferta de produtos formalmente autorizados. Também está prevista a harmonização com guias técnicos de agências de referência internacionais.
– Comunicação com a sociedade: elaboração de plano de comunicação em linguagem simples sobre os riscos do uso indiscriminado, identificação de produtos irregulares, limites da manipulação magistral e campanhas direcionadas a pacientes e profissionais de saúde.
– Governança: criação de grupo interno para monitorar e avaliar a implementação das medidas e promover ajustes contínuos.
A proposta de revisão da nota técnica está em elaboração e será debatida na reunião da diretoria colegiada da Anvisa marcada para o dia 15.